

微信扫描二维码,即可将本页分享到“朋友圈”中。

2026-01-09 来源:中集中电作者:孔小萍 浏览数:185
在绿色能源转型的浪潮中,水电解制氢作为连接可再生能源与终端应用的关键桥梁,正受到前所未有的关注。作为深耕以水电解制氢设备
在绿色能源转型的浪潮中,水电解制氢作为连接可再生能源与终端应用的关键桥梁,正受到前所未有的关注。作为深耕以水电解制氢设备研发与制造为代表的氢基能源企业,中集中电始终聚焦于这一核心技术的突破与产业化应用。今天,我们将与您一同潜入电解水的微观秘境,解锁原子与电子间协同运作的反应密码,探寻这项承载着百年积淀的技术,何以在当下成为推动能源革命的关键力量,以及我们如何通过持续创新,在这场“分子舞蹈”中扮演重要的编排者与推进者。
核心原理
一次“电子搬家”驱动的分子拆解
电解水的本质,是电能驱动下的、非自发的化学反应。水分子(H₂O)本身非常稳定,要拆开它需要能量。电解过程,就是通过外加电场,为水分子提供能量,并引导电子(e-)完成一次精准的“定向搬迁”,从而拆解分子。它的总反应式看似简单:
2H₂O → 2H₂ + O₂
但在这个宏观现象之下,是两个精心设计、在不同电极表面独立进行的半反应。这两个反应被离子导体(电解液)连接,共同构成一个完整的电荷与物质循环。
阴极——氢气的“诞生地”
析氢反应(HER)作为电解水的阴极反应,其理论电势为0 V,但实际应用中往往涉及多余的能量损耗,需要引入活化能促使析氢反应发生。
HER的动力学主要包括两个步骤:
(1)吸附氢原子(H*)的形成(Volmer);
(2)H*的伴随结合生成H2分子(Heyrovsky或者Tafel)。
不同的反应环境具有不同的反应路径,如下所示:
酸性电解液中:
H3O+ + e- + * → H* + H₂O(Volmer)(1-2)
H+ + e- +H* → H₂(Heyrovsky)(1-3)
或2 H* → H₂(Tafel)(1-4)
中性和碱性电解液中:
H₂O + e- → OH- + H*(Volmer)(1-5)
H* + e- + H₂O → H₂ + OH-(Heyrovsky)(1-6)
或2 H* → H₂(Tafel)(1-7)
对比不同介质中的析氢机理,可发现酸性或碱性条件下均会发生Volmer反应,而氢脱附反应则由催化剂性能决定。综上所述,析氢反应机制为Volmer-Heyrovsky和Volmer-Tafel两种过程。
阳极——更复杂、更关键的“瓶颈”
析氧反应(OER)是电催化分解水过程中的关键步骤,目前普遍认为其存在两种主要机理,其中一种是较为传统的吸附物主导机制(AEM),该机制通过过渡金属活性中心上的协同电子–质子转移序列进行。在这一机制中,中间体M-OH最初由氢氧根离子(OH-)在单电子氧化作用下于表面金属位点(M)上形成,并作为催化活性位点。随后,M-OH经过电子转移和质子耦合步骤转化为M-O。当氢氧根离子再次经历单电子氧化时,M-O进一步转化为M-OOH,最终通过另一个电子转移和质子耦合过程生成O2。AEM过程在酸性和碱性条件下的OER反应机理存在显著差异。
在酸性条件下:
H₂O + * → OH* + H+ + e- (2−1)
OH* → O* + H+ + e– (2−2)
O* + H₂O → OOH* + H+ + e– (2−3)
OOH* → O₂* + H+ + e– (2−4)
O₂* → O₂ + * (2−5)
总反应为:2H₂O → O₂ + 4H+ + 4e– (2−6)
在碱性条件下:
OH– → OH* + e– (2−7)
OH* → O* + H+ + e– (2−8)
2O* → O₂ + * (2−9)
总反应为:4OH– → O₂ + 2H₂O + 4e– (2−10)
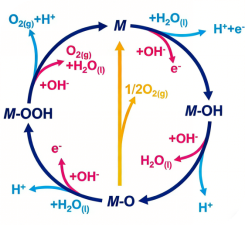
图1 OER反应机理(其中红线为酸性OER过程,浅蓝线为碱性OER过程,深蓝线表示两个相邻的M–O直接生成氧气的过程)
相较于传统吸附演化机制,近年来兴起的晶格氧介导机制(LOM)为OER机理研究开辟了全新视角。与AEM不同,LOM机制指出,OER过程中生成的氧气既可能源自电解液中的水分子,也可能由催化剂晶格氧原子直接参与O-O键构建而来。这一创新机制打破了AEM的传统理论框架,为阐释部分固相催化剂展现出的超高催化活性提供了更贴合实际的理论支撑。
从反应动力学角度分析,LOM机制突破了AEM中O-O键形成这一决速步的制约,进而呈现出显著的动力学优势。相关研究数据表明,基于LOM机制的OER催化性能较传统AEM机制提升3~5倍,充分彰显了该机制在催化效率提升方面的突破性价值。需要强调的是,LOM机制的具体反应路径会随电解液环境的改变而发生适应性调整。
在酸性体系中,水分子更易吸附于催化剂表面氧空位邻近的金属活性位点,随后通过作用于氧空位实现晶格氧的活化,最终完成O-O键的形成与氧气释放,同时实现氧空位的再生循环。而在碱性环境下,羟基离子首先吸附于氧空位附近的金属位点,紧接着另一个羟基离子在氧空位处发生脱氢反应,最终借助氧空位的介导作用形成O-O键并释放氧气。无论处于酸性还是碱性体系,LOM机制的核心特征均为催化剂晶格氧直接参与OER反应进程,而非依赖表面吸附中间体的转化过程。这一独特特性不仅为深入理解OER反应本质提供了全新的理论维度,更为高效OER催化剂的设计提供了新思路。通过精准调控催化剂的晶格氧活性,有望进一步优化OER 反应动力学性能,从而助力水电解制氢技术迈向实用化新阶段。
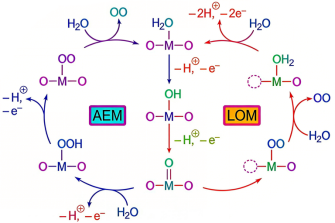
图2 吸附析出机理(AEM)和晶格氧机理(LOM)示意图
纯水在25°C下的理论分解电压是1.23 V。从热力学上看,这意味着只要提供高于1.23 V的电压,反应就应发生。但在现实中,电解槽的实际工作电压通常高达1.8-2.2V,甚至更高。这多出来的部分,就是能量损耗,主要来自:
过电位:克服电极反应能垒所需的“额外推力”,尤其是阳极的析氧反应过电位最高,中性电解液的过电位显著高于酸性和碱性。
欧姆损耗:电解液、连接部件的自身电阻导致的发热损耗,中性电解液的欧姆损耗通常最大(离子浓度低、传导效率差)。
未来方向:从核心突破到多元创新
基于原理的深刻瓶剖析,指明了技术进化的三大核心方向,既直击现存痛点,又拓展应用边界:
1.催化剂革新:突破“高过电位”与“高成本”双重枷锁
当前电解水制氢的核心瓶颈之一,是阳极析氧反应的高过电位和贵金属催化剂的依赖。未来研发将聚焦开发非贵金属催化剂,如过渡金属氧化物、硫化物、磷化物等,通过调控晶体结构、电子态和活性位点,提升催化活性与稳定性,替代铱、钌等稀有贵金属,大幅降低材料成本。
2.海水电解制氢:破解“淡水资源依赖”难题
全球淡水资源稀缺,而海水储量丰富,海水电解制氢是实现氢能规模化应用的关键路径。
3.电解水制氢耦合氧化:实现“制氢+高值产物”双赢
传统电解水阳极仅发生析氧反应,产物单一且能耗偏高。未来可通过“耦合氧化反应”重构阳极过程:用低能垒的有机小分子氧化(如甲醇、乙二醇、甘油氧化)、生物质氧化或工业废水中污染物氧化,替代高能耗的析氧反应。此举不仅能降低阳极过电位,减少整体电解能耗,还能同步生成甲醛、乙醛、有机酸等高附加值化学品,或实现废水无害化处理。让电解水制氢从“单一产氢”升级为“能源与资源协同利用”的多元系统。
总结
从外加电场驱动电子迁移,到离子在电解质中穿梭完成电荷循环,再到催化剂表面精准的分子键断裂与重组——电解水制氢,是一场在微观尺度上被精密编排的“分子舞蹈”。理解它,不仅让我们惊叹于科学的力量,更能看清技术突破的方向。
中集中电,正是这场“分子舞蹈”的坚定实践者与创新者。我们通过持续深化对基础机理的理解,将原理层面的认知转化为与核心供应商在电极、催化剂、膜材料乃至整机系统的共同创新设计。当绿色电力驱动这场舞蹈规模化、多元化上演时,我们期待以更高效、更经济、更可靠的制氢设备,助力氢能真正成为全球能源转型的核心支柱。探索不息,创新不止,中集中电与您一同见证并推动绿色氢能时代的到来。
中集中电提供以碱性水电解制氢为主的氢基能源全套设备,包括集装箱化撬装制氢工厂、中压电解槽、常压电解槽、BOP 系统,产品覆盖10Nm³/h~4000Nm³/h 全系列;提供合成氨、合成甲醇等化工撬装模块,产品覆盖 1kt/a~50kt/a;提供风光绿电+储能+制氢合成氨/合成甲醇/冶金、制加氢一体站、海上能源岛等一体化解决方案,包括系统配置、经济测算、运行策略等。提供水电解制氢项目专业运维服务,包括设备调试运行、检修维护、全生命周期设备健康管理等。

版权与免责声明:
凡注明稿件来源的内容均为转载稿或由企业用户注册发布,本网转载出于传递更多信息的目的,如转载稿涉及版权问题,请作者联系我们,同时对于用户评论等信息,本网并不意味着赞同其观点或证实其内容的真实性;
本文地址:http://www.h2fc.net/Technology/show-4294.html
转载本站原创文章请注明来源:中国氢能与燃料电池网

氢能与燃料电池产业
微信扫描关注
